
近几年外泌体研发持续升温,全球科研大咖纷纷扎堆此领域,有关外泌体载药、诊断、免疫疗法等方向的文章陆续发表在Science、Nature等各大顶级期刊上,外泌体已成为生命科学/基础医学研究的一大热点。


图片来自期刊
外泌体是由哺乳动物细胞主动向胞外和体液中释放的纳米级双层囊泡小体,携带多种遗传物质,可通过自分泌或旁分泌途径被细胞吸收,也可经循环系统被远距离靶组织或器官所吸收,能参与机体多种生理和病理过程。

外泌体于1983年首次在体外培养的绵羊红细胞上清液中发现且能被多种细胞分泌。最初外泌体被认为是细胞成熟过程中调节膜功能而释放的多余膜蛋白,是清除细胞碎片和淘汰细胞表面分子的细胞器。后来越来越多的研究发现,外泌体在介导炎症反应、细胞增殖、调节细胞外微环境和诱导机体免疫反应等方面都发挥着重要作用。
如今,外泌体被认为是疾病的生物标志物和预后因子,另外还有潜力作为基因和药物递送的载体,具有重要的临床意义。
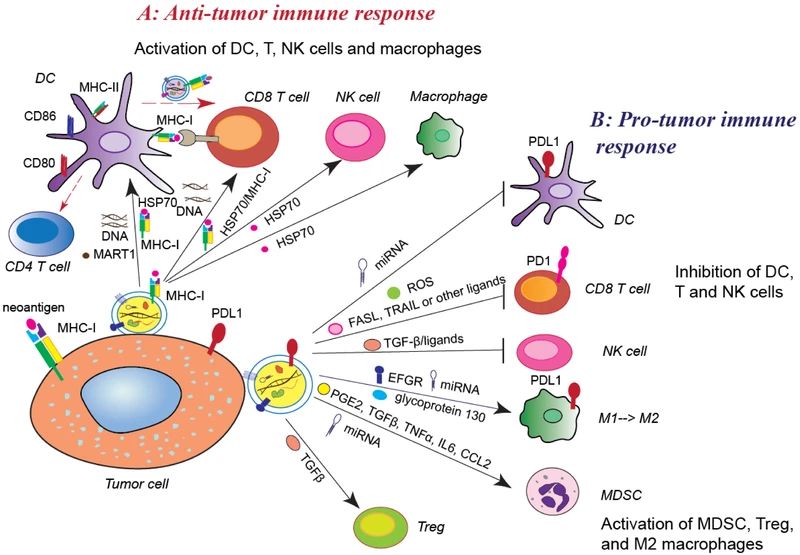
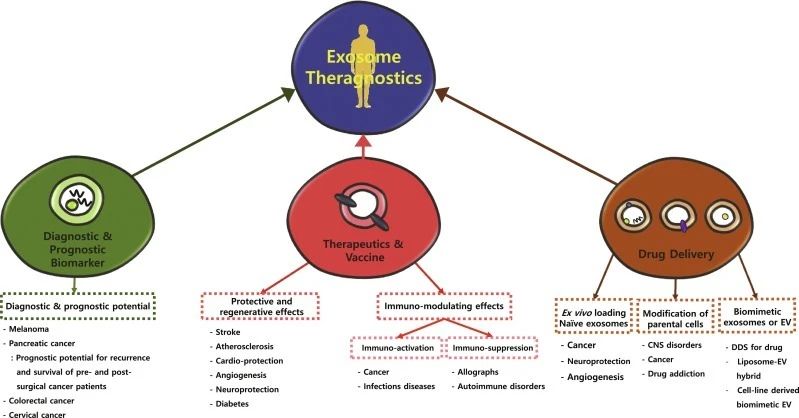
02外泌体作为药物输送系统 外泌体由于其表面具有多种粘附蛋白已经成为基因治疗的潜在载体,纳米尺寸和柔韧性使它们能够跨越主要的生物屏障,如血脑屏障(BBB)等。 与脂质体制剂相反,外泌体是天然存在的分泌性膜囊泡,毒性较低,从它们在体内普遍存在可以推断出其在体内的耐受性很好。另外,外泌体固有的归巢能力暗示了它们在药物递送中的潜在效用。例如,源自黑色素瘤的外泌体优先进入前哨淋巴结,这种归巢能力可以用作药物的靶向递送。 Alvarez-Erviti等人研究发现DC衍生的外泌体可将siRNA传递给小鼠的大脑,继而推断出外泌体加载的药物或siRNA可以通过BBB。他们首先转导DC以表达外泌体膜蛋白LAMP2B,该蛋白能与神经元特异性RVG肽融合。纯化的DC外泌体中装有靶向BACE1(阿尔茨海默病的发病机理中的重要调控基因)的外源siRNA,然后将这些iExosome静脉注射到小鼠体内。这些外泌体特异性进入大脑中的神经元、小胶质细胞和少突胶质细胞,导致小鼠模型中BACE1基因敲低。这项研究证明了外泌体特异性全身递送的可行性,更重要的是,该研究表明外泌体可以通过生物屏障,表明了基于RNAi的新型脑肿瘤、脑转移瘤治疗的可能性。 外泌体天然适于运输蛋白质、mRNA、miRNA、各种非编码RNA、线粒体DNA以及基因组DNA,这使得它们可用于递送干扰RNA以及其他治疗性物质(如亲脂性小分子),已有研究将抗炎剂姜黄素、抗癌剂阿霉素和紫杉醇等装载到外泌体囊泡中用于相应疾病的治疗。基于外泌体的药物递送系统由于其内源性在癌症的治疗中具有极大优势,能使得免疫原性和毒性最小化。例如,一些研究表明,与其他递送系统相比,加载到外泌体中的阿霉素的治疗功效大大增强,并且对主要器官系统(尤其是心脏)的不良影响明显减少。 03 外泌体作为癌症免疫疗法 最近,免疫检查点疗法在几种癌症类型中的成功提高了人们对进一步探索肿瘤中免疫失调的兴趣,其中包括外泌体肿瘤免疫疗法,有望诞生抗癌疫苗。 04 外泌体的抑制 外泌体水平升高通常与不同类型的癌症恶化相关,一些研究人员希望能通过降低肿瘤外泌体到正常水平来防止不良预后。 从这个角度出发,许多正在进行的研究旨在通过调节外泌体生成分泌的过程或通过特异性靶向其成分抑制其与靶细胞的相互作用来调节外泌体的产生。 参考文献 1. H Rashed, M., Bayraktar, E., K Helal, G., Abd-Ellah, M. F., Amero, P., Chavez-Reyes, A., & Rodriguez-Aguayo, C. (2017). Exosomes: From Garbage Bins to Promising Therapeutic Targets. International journal of molecular sciences,18(3),538. https://doi.org/10.3390/ijms18030538 2. Zhang, L., & Yu, D. (2019). Exosomes in cancer development,metastasis,and immunity. Biochimica et biophysica acta. Reviews on cancer,1871(2),455–468. https://doi.org/10.1016/j.bbcan.2019.04.004 3. Kang J. S. (2020). The potential of exosomes as theragnostics in various clinical situations.Exosomes,467–486. https://doi.org/10.1016/B978-0-12-816053-4.00020-1 4. Gurunathan, S., Kang, M. H., Jeyaraj, M., Qasim, M., & Kim, J. H. (2019). Review of the Isolation, Characterization, Biological Function, and Multifarious Therapeutic Approaches of Exosomes.Cells,8(4),307. https://doi.org/10.3390/cells8040307 5. 吴金恩, & 丁军涛. (2016). 外泌体生物学功能及应用研究进展. 动物医学进展, 037(012), 90-94. 6. 吴奇, 杨国栋, 韦梦影, 马雪, & 陈辉. (2016). 外泌体的生物学功能及其在基因治疗中的应用. 现代生物医学进展(34), 6785-6788. 免责声明:我们尊重原创,也注重分享。部分素材来源网络,版权归原作者所有,如有侵权请联系删除。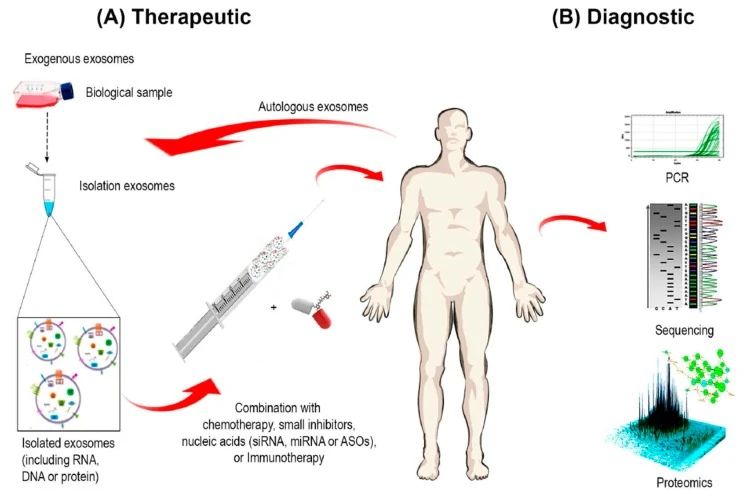
上一篇:点赞!北京首张CAR-T细胞治疗产品生产许可证获批!中国药谷
下一篇:暂无